Микробиота кишечника – один из ключевых регуляторов метаболических заболеваний
Л.Н. Костюченко [1] *, https://orcid.org/0000-0003-3084-7563, l.kostyuchenko@mknc.ru
Т.А. Васина [2], https://orcid.org/0000-0001-8912-4111, aa221947@yandex.ru
А.Э. Лычкова [1], https://orcid.org/0000-0002-3856-275X, a.lychkova@mknc.ru
1. Московский клинический научный центр имени А.С. Логинова; 111123, Россия, Москва, шоссе Энтузиастов, д. 86
2. Научно-исследовательский институт скорой помощи имени Н.В. Склифосовского; 129090, Россия, Москва, Большая Сухаревская пл., д. 3
Резюме
Введение. Наличие у пациента ожирения или, наоборот, недостаточности питания сопровождается различными метаболическими нарушениями и находится в центре внимания современной медицинской науки и организаторов здравоохранения.
Цель. Раскрыть механизм действия (воздействие на моторику посредством кишечной микробиоты) препарата мебеверин в структуре сопутствующей метаболической терапии у пациентов с различной массой тела (различной нутриционной недостаточностью).
Материалы и методы. Обследованы 38 чел. с различной массой тела (от 38 до 135 кг). Предложен индекс нутриционной недостаточности (ИНН), который рассчитывался нами на основе параметров алиментационно-волемического диагноза (АВД) и выражался в баллах: до 29 баллов – легкая степень нутриционной недостаточности (риск операции минимальный, операция возможна после кратковременной инфузионной подготовки);
29–30 – средняя степень (риск относительно высокий, операция возможная только после хотя бы минимальной предварительной инфузионно-алиментационной коррекции);
31–33 – тяжелая степень нутриционной недостаточности (риск операции высокий, выполнять операцию можно лишь экстренную после минимальной подготовки либо плановую после длительной подготовки пациента к операции до повышения нутриционного статуса на 1–2 уровня;
34–42 – крайне тяжелая (только экстренные операции либо паллиатив после предварительной подготовки, поднятие по возможности нутриционного статуса на 1–2 уровня). Реабилитационный потенциал определяли по общепринятым формулам, микробиоту – по уровню выделяемых ею метаболитов. Электрическую активность и по ней характер моторики выясняли с помощью мингографа.
Результаты и обсуждение. При обследовании выявили, что при различной нутриционной недостаточности микробиота разнится. При 29–30 баллах возникают нутриционная недостаточность и высокий реабилитационный риск. Реабилитационный потенциал имеет 4 уровня оценки. Высокий реабилитационный потенциал предполагает возможность достижения полного восстановления здоровья.
Выводы. Микробиота кишечника – ключевой регулятор метаболических заболеваний. При приеме мебеверина целесообразно применять детоксикационную коррекцию, так как он метаболизируется в печени. Не вызывает сомнения важность дальнейшего исследования состояния микробиоты в современном мире при различном ИНН.
Ключевые слова: микробиота кишечника, мебеверин, нутриционная недостаточность, моторика кишечника, реабилитационный потенциал.
Для цитирования: Костюченко Л.Н., Васина Т.А., Лычкова А.Э. Микробиота кишечника – один из ключевых регуляторов метаболических заболеваний. Медицинский совет. 2022;16(23):174–179. https://doi.org/10.21518/2079-701X-2022-16-23-174-179. Конфликт интересов: авторы заявляют об отсутствии конфликта интересов.
ВВЕДЕНИЕ
Наличие ожирения или, наоборот, недостаточности питания сопровождается различными метаболическими нарушениями [1–6] и находится в центре внимания современной медицинской науки и организаторов здравоохранения [7–10]. Особенно актуален для клиницистов поиск новых показателей для прогнозирования развития метаболических сдвигов у пациентов с избыточной массой тела. В целом лечению функциональных и метаболических заболеваний кишечника посвящено значительное число исследований, сопровождающихся сопутствующей терапией, как в России, так и за рубежом [11–18]. В решении данной проблемы в значительной степени помогает сопутствующая терапия нутриционных сдвигов [15–21]. Один из препаратов сопутствующей коррекции – отечественный мебеверин (Спарекс®).
Цель настоящей работы – раскрыть еще один механизм действия (воздействие на моторику посредством кишечной микробиоты) препарата мебеверин в структуре сопутствующей терапии синдрома раздраженного кишечника.
МАТЕРИАЛЫ И МЕТОДЫ
Обследованы 38 чел. с различной массой тела (от 38 до 135 кг). Предложен индекс нутриционной недостаточности (ИНН) [22], который рассчитывался нами на основе параметров алиментационно-волемического диагноза и выражался в баллах:
■ до 29 баллов – легкая степень нутриционной недостаточности (НН): риск операции минимальный, операция возможна после кратковременной инфузионной подготовки;
■ 29–30 – средняя степень: риск относительно высокий, операция возможная только после хотя бы минимальной предварительной инфузионно-алиментационной коррекции;
■ 31–33 – тяжелая степень НН: риск операции высокий, выполнять операцию можно лишь экстренную после минимальной подготовки либо плановую после длительной подготовки пациента к операции до повышения нутриционного статуса на 1–2 уровня;
■ 34–42 – крайне тяжелая: только экстренные операции либо паллиатив после предварительной подготовки, подняв по возможности нутриционный статус на 1–2 уровня.
Повышенную массу тела оценивали с помощью индекса массы тела. Реабилитационный потенциал (РП) определяли по общепринятым формулам. Микробиоту определяли также традиционным методом [23]. Электрическую активность и по ней характер моторики выясняли с помощью мингографа [21, 22, 24]. РП – комплекс биологических, психофизиологических характеристик человека, а также социально-средовых факторов, позволяющих в той или иной степени реализовать его потенциальные способности с их оценкой: РП высокий, удовлетворительный, низкий.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Европейское общество клинического питания и метаболизма (ESPEN) для оценки нутритивного статуса пациентов рекомендует использовать систему «Оценка нутриционного риска» (Nutritional Risk Screening – NRS). Американское общество парентерального и энтерального питания (ASPEN) рекомендует использовать опросник «Глобальная субъективная оценка пациентов» (Patient Generated Subjective Global Assessment – PGSGA, чаще просто SGA). Однако обе системы обладают рядом недоговоренностей.
У обследуемых пациентов определяли ИНН, РП и связанный с ним реабилитационный риск (РР). При обследовании выявили, что при различной НН микробиота разнится. При 29–30 баллах возникают НН и высокий РР.
У пациентов с избыточной массой тела НН выражается в диспропорциях как в параметрах состава тела, так и в соотношениях метаболитов микробиоты кишечника. Это может быть связано с особенностями проживания в современном мире (наличие искусственных радиационных поясов вокруг Земли, особенностей алиментации и пр.). Асимметричные ответы ведут к тому, что эффективность защитных механизмов не снижается. Однако все это требует дальнейшего более глубокого изучения в связи с возможностями РП.
РП имеет 4 уровня оценки:
■ высокий предполагает возможность достижения полного восстановления здоровья, всех обычных для инвалида видов деятельности, в том числе способности к трудовой деятельности, и социального положения (полная реабилитация);
■ средний отмечается при неполном выздоровлении с остаточными проявлениями в виде выраженного нарушения функций. Выполнение основных видов деятельности возможно в ограниченном объеме или с помощью технических либо иных средств реабилитации, отмечается частичное восстановление трудоспособности при сохранении частичного снижения уровня и качества жизни, потребности в социальной помощи и защите (частичная реабилитация – переход из I и II группы инвалидности в III группу);
■ низкий отмечается при медленно прогрессирующем течении заболевания, выраженном нарушении функций, значительных ограничениях жизнедеятельности, включая способность к трудовой деятельности, потребности в постоянной социальной помощи и защите (переход из I группы инвалидности во II группу);
■ отсутствие РП наблюдается при прогрессирующем течении заболевания, резко выраженном нарушении функций органов и систем, невозможности компенсации ограничений жизнедеятельности, наличии стойкой частичной или полной утраты трудоспособности, необходимости в постоянном постороннем уходе или надзоре, потребности в постоянной социальной помощи и защите (реабилитация невозможна – стабильная инвалидность или ее утяжеление).
Всем пациентам назначалась корригирующая терапия. Сопутствующая терапия была направлена на нутритивную коррекцию, коррекцию нутритивного статуса и двигательной функции кишечника. При этом двигательную функцию желудочно-кишечного тракта удавалось регулировать (до 29 баллов ИНН) с помощью сопутствующей терапии, в частности, мебеверином (рис. 1).
Известно, что при приеме внутрь мебеверин подвергается пресистемному гидролизу и не обнаруживается в плазме. Метаболизируется в печени до вератровой кислоты и мебеверинового спирта. Выводится главным образом почками в виде метаболитов, в небольших количествах – желчью (рис. 2). Капсулы мебеверина имеют свойство продолжительного высвобождения, что весьма целесообразно. Важно, что даже после многократного приема не наблюдается значительной кумуляции.
Мебеверин представляет собой капсулы или двояковыпуклые таблетки, покрытые пленочной оболочкой, белого или почти белого цвета. Допустима незначительная шероховатость поверхности. На поперечном разрезе ядро таблетки белого или почти белого цвета.
При сравнении данных спектра микробиоты у пациентов с различным ИНН выявлено следующее. В связи с тем, что данный препарат метаболизируется печенью, целесообразно, по-видимому, параллельно обеспечивать детоксикацию. Механизмы детокс-препаратов различны. Так, при нарушениях пищеварения, синтеза можно ориентироваться на Фосфонциале, Эксхол и др. (рис. 1).
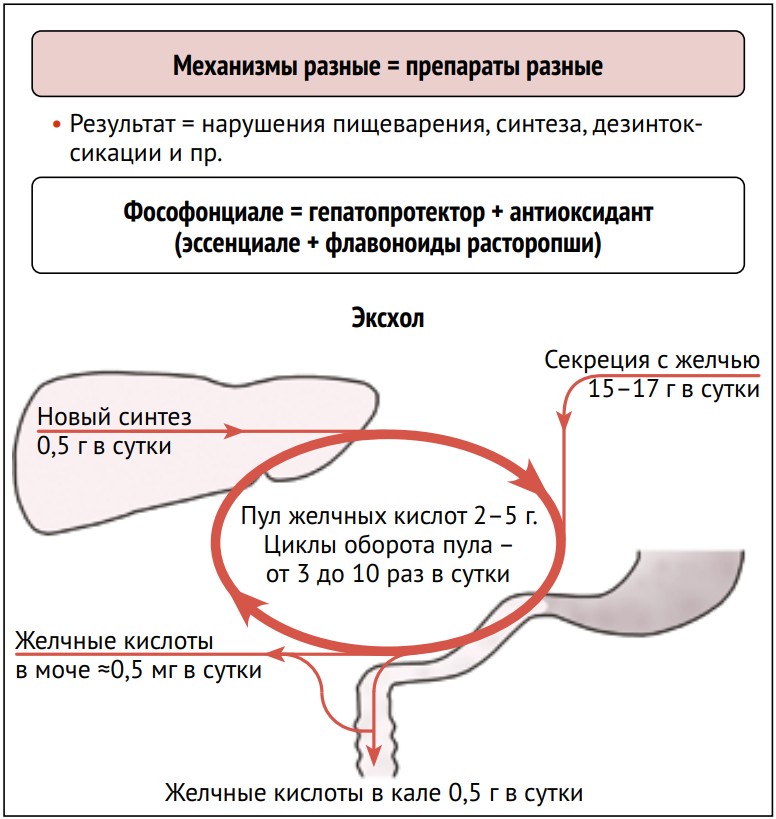
Рисунок 1. Механизм действия некоторых детокс-препаратов

Рисунок 2. Механизм детоксикации, связанный с метаболизмом желчных кислот и мебеверинового спирта Эффективность такого лечебного подхода приведена на рис. 3 [25].
 коррекции метаболизма [25].jpg)
Рисунок 3. Эффективность мебеверина в структуре комплексной (с ремаксолом) коррекции метаболизма [25]
Таким образом, при коррекции нутриционных сдвигов необходимо проводить комплексное лечение. При этом важно учитывать механизм действия микробиоты и использовать препараты, направленные на регуляцию моторики через ее посредничество. В частности, для этого целесообразно применять мебеверин (рис. 3) в стандартных дозировках в структуре нутриционного воздействия [25–30]. Полученные данные свидетельствуют о возрастающем интересе ученых к более детальному изучению влияния микробиоты на разные патологические состояния человека. Дальнейшее изучение позволит диагностировать различные заболевания человека, их связь с микробиотой, а также разработать новые эффективные методы терапии различных заболеваний с нарушением массы тела.
ВЫВОДЫ
■ Микробиота кишечника – ключевой регулятор метаболических заболеваний.
■ При приеме мебеверина (Спарекс®) целесообразно применять детоксикационную коррекцию, так как он метаболизируется в печени.
■ Не вызывает сомнения целесообразность дальнейшего исследования состояния микробиоты в современном мире при различном ИНН.
■ Терапевтическая эффективность коррекции дисфункций желудочно-кишечного тракта зависит от точности диагностики патологии, применения селективных препаратов и последующих лечебных мер. Полученные данные свидетельствуют о возрастающем интересе ученых к более детальному изучению влияния микробиоты на разные патологические состояния человека, что позволит более тонко и эффективно диагностировать различные обменные заболевания человека, их связь с микробиотой, а также разработать новые эффективные методы терапии для восстановления эубиоза, ликвидации вторичного иммунодефицита, сопровождающего избыточную массу тела.
Список литературы
1. Кошимбетова Г.К., Кутлимуратова З.Р. Синдром раздраженного кишечника как аспект функциональных заболеваний желудочно-кишечного тракта. Medicus. 2019;(2):35–37. Режим доступа: https://elibrary.ru/item.asp?id=39385763.
2. Андреев Д.Н. Роль нарушения проницаемости слизистой оболочки кишечника в генезе функциональных заболеваний желудочнокишечного тракта. Consilium Medicum. 2019;21(8):29–34. Режим доступа: https://consilium.orscience.ru/2075-1753/article/view/96779.
3. Степанов Ю.М., Федорова Н.С., Зигало Э.В. Эффективность рифаксимина в коррекции синдрома избыточного бактериального роста при хронических воспалительных и функциональных заболеваниях кишечника. Гастроентерологiя. 2019;53(4):246–251. Режим доступа: https://cyberleninka.ru/article/n/effektivnost-rifaksimina-v-korrektsii-sindroma-izbytochnogobakterialnogo-rosta-pri-hronicheskih-vospalitelnyh-i-funktsionalnyh.
4. Андреев Д.Н., Дичева Д.Т. Нарушение проницаемости слизистой оболочки кишечника как фактор этиопатогенеза функциональных заболеваний желудочно-кишечного тракта. Медицинский совет. 2020;(5):87–95. https://doi.org/10.21518/2079-701X-2020-5-87-95.
5. Минушкин О.Н., Масловский Л.В., Буланова М.И., Гордиенко Е.С., Топчий Т.Б., Бейлина Н.И. Опыт применения метапребиотиков в лечении некоторых функциональных заболеваний кишечника. Медицинский совет. 2020;(15):105–111. https://doi.org/10.21518/2079-701X-2020-15-105-111.
6. Погодина А.А., Романица А.И., Рычкова Л.В. Ожирение и функциональные заболевания кишечника: существует ли связь? Ожирение и метаболизм. 2021;18(2):132–141. https://doi.org/10.14341/omet12706.
7. Кондрашова Е.А., Парфёнов А.И. Активность дисахаридаз в норме и у пациентов с функциональными заболеваниями кишечника. Доктор.Ру. 2021;20(4):55–60. https://doi.org/10.31550/1727-2378-2021-20-4-55-60.
8. Ивашкин К.В., Гречишникова В.Р., Решетова М.С., Ивашкин В.Т. Связь синдрома раздраженного кишечника и синдрома избыточного бактериального роста: бактериальная гипотеза в основе функционального заболевания. Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2021;31(1):54–63. https://doi.org/10.22416/1382-4376-2021-31-1-54-63.
9. Минушкин О.Н., Масловский Л.В., Ардатская М.Д., Буланова М.И., Бейлина Н.И., Колодкин А.М. и др. Клинико-метаболические эффекты терапии метапребиотиками некоторых функциональных заболеваний кишечника. Экспериментальная и клиническая гастроэнтерология. 2021;(10):100–108. https://doi.org/10.31146/1682-8658-ecg-194-10-100-108.
10. Минушкин О.Н., Масловский Л.В., Фролова А.А., Шиндина Т.С., Буланова М.И., Легкова К.С. Применение комбинированного растительного препарата при некоторых функциональных заболеваниях кишечника – реализация концепции мультитаргетной терапии. Экспериментальная и клиническая гастроэнтерология. 2022;(9):82–88. https://doi.org/10.31146/1682-8658- ecg-205-9-82-88.
11. Чуркова М.Л., Костюкевич С.В. Эпителий слизистой оболочки толстой кишки в норме и при функциональных и воспалительных заболеваниях кишечника. Экспериментальная и клиническая гастроэнтерология. 2018;(5):128–132. Режим доступа: https://www.nogr.org/jour/article/view/624.
12. Парфенов А.И., Дбар С.Р., Ахмадуллина О.В., Сабельникова Е.А., Крумс Л.М., Быкова С.В., Белостоцкий Н.И. Дисахаридазная недостаточность под маской функционального заболевания кишечника. Доказательная гастроэнтерология. 2018;7(1):57. https://doi.org/10.17116/dokgastro20187155-110.
13. Маев И.В., Казюлин А.Н., Андреев Д.Н. Состояние сердечно-сосудистой системы у пациентов с функциональными и воспалительными заболеваниями кишечника. Терапевтический архив. 2018;90(2):59–64. https://doi.org/10.26442/terarkh201890259-64.
14. Успенский Ю.П., Гнутов А.А., Фоминых Ю.А., Мирзоев О.С. Современная парадигма функциональных заболеваний желудочно-кишечного тракта: фокус внимания на функциональную диспепсию, дисфункцию сфинктера Одди и синдром раздраженного кишечника. Медицинский алфавит. 2019;3(20):24–29. https://doi.org/10.33667/2078-5631-2019-2-20(395)-24-29.
15. Ивашкин К.В., Решетова М.С., Зольникова О.Ю., Корнеева В.Р., Широкова Е.Н. Место пробиотиков в комплексной терапии различных заболеваний желудочно-кишечного тракта. Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2020;30(1):42–48. https://doi.org/10.22416/1382- 4376-2020-30-1-42-48.
16. Успенский Ю.П., Мирзоев О.С. Клинико-психологическая характеристика больных с сочетанием функциональной диспепсии и синдрома раздраженного кишечника: результаты собственного исследования. Университетский терапевтический вестник. 2022;4(1):22–31. https://doi.org/10.56871/2945.2022.92.72.003.
17. Комиссаренко И.А., Левченко С.В. Нарушение функции кишечника у пациентов с метаболическим синдромом. Лечащий врач. 2022;(7-8):62–70. https://doi.org/10.51793/OS.2022.25.8.010.
18. Успенский Ю.П., Мирзоев О.С., Фоминых Ю.А., Иванов С.В. Современный взгляд на проблему сочетанных функциональных заболеваний органов пищеварения. Медицинский алфавит. 2018;1(7):42–47. Режим доступа: https://www.med-alphabet.com/jour/article/view/559.
19. Киреева Т.И. Особенности вегетативного тонуса больных с синдромом раздраженного кишечника. Современные научные исследования и разработки. 2018;(10):415–417. Режим доступа: https://elibrary.ru/item.asp?id=36482604.
20. Клименко Е.С., Белькова Н.Л., Погодина А.В., Рычкова Л.В., Даренская М.А. Коморбидность функциональных расстройств кишечника и ожирения с точки зрения микробиом. Acta Biomedica Scientifica. 2022;7(5-2):56–66. https://doi.org/10.29413/ABS.2022-7.5-2.6.
21. Якупова А.А., Абдулхаков С.Р., Залялов Р.К., Сафин А.Г., Абдулхаков Р.А. Методы оценки кишечной проницаемости: обзор литературы. Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2021;31(1):20–30. https://doi.org/10.22416/1382-4376-2021-31-1-20-30.
22. Костюченко Л.Н. (ред.). Нутрициология в гастроэнтерологии. М.: МК; 2013. 431 с.
23. Сидоренко О.О., Жукова Е.Е., Иванов А.А., Костюченко Л.Л. Ситология и лактотерапия. М.: ИНФРА-М; 2022. 218 с. https://doi.org/10.12737/1852468.
24. Лычкова А.Э., Ручкина И.Н., Полева Н.И., Пузиков А.М. Моторная функция кишечника при синдроме раздраженной кишки с запорами. Экспериментальная и клиническая гастроэнтерология. 2019;(2):75–78. https://doi.org/10.31146/1682-8658-ecg-162-2-75-78.
25. Мазина Н.К., Мазин П.В., Суханов Д.С. Клиническая эффективность сукцинатсодержащего инфузионного препарата при фармакотерапии поражений печени разного генеза: результаты метаанализа. Терапевтический архив. 2013;(1):56–61. Режим доступа: https://cyberleninka.ru/article/n/klinicheskaya-effektivnost-suktsinatsoderzhaschego-infuzionnogopreparata-pri-farmakoterapii-porazheniy-pecheni-raznogo-geneza?ysclid=l c67qyk423551273750.
26. Шилов В.В., Шикалова И.А., Васильев С.А., Лоладзе А.Т., Батоцыренов Б.В. Особенности фармакологической коррекции токсических поражений печени у больных с синдромом зависимости от алкоголя и тяжелыми формами острых отравлений этанолом. Журнал неврологии и психиатрии им. С.С. Корсакова. 2012;112(1):45–48. Режим доступа: https://www.elibrary.ru/item.asp?id=17911807
27. Суханов Д.С., Иванов А.К., Романцов М.Г., Коваленко А.Л. Лечение гепатотоксических осложнений противотуберкулезной терапии сукцинатсодержащими препаратами. Российский медицинский журнал. 2012;(6):22–25. Режим доступа: https://www.elibrary.ru/item.asp?id=13361786.
28. Сологуб Т.В., Горячева Л.Г. Гепатопротективная активность ремаксола при хронических поражениях печени (материалы многоцентрового рандомизированного плацебо-контролируемого исследования). Вестник Северо-Западного государственного медицинского университета им. И.И. Мечникова. 2009;(2):1–8.
29. Сологуб Т.В., Горячева Л.Г., Суханов Д.С., Романцов М.Г., Антонова Т.В., Яковлев А.А. и др. Гепатопротективная активность ремаксола при хронических поражениях печени. Клиническая медицина. 2010;(1):62—66. Режим доступа: http://elib.fesmu.ru/elib/Article.aspx?id=217319.
30. Стельмах В.В., Козлов В.К., Радченко В.Г., Некрасова А.С. Патогенетическая терапия метаболического синдрома на стадии органных поражений. Клиническая медицина. 2012;(6):61–65. Режим доступа: https://cyberleninka. ru/article/n/patogeneticheskaya-terapiya-metabolicheskogo-sindroma-nastadii-organnyh-porazheniy/viewer.
Информация об авторах:
• Костюченко Людмила Николаевна, академик РАЕ, д.м.н., профессор, заведующий лабораторией нутрициологии, Московский клинический научно-практический центр имени А.С. Логинова; 111123, Россия, Москва, шоссе Энтузиастов, д. 86; l.kostyuchenko@mknc.ru• Васина Татьяна Афанасьевна, д.м.н., профессор, ведущий научный сотрудник, Научно-исследовательский институт скорой помощи имени Н.В. Склифосовского; 129090, Россия, Москва, Б. Сухаревская пл., д. 3; aa221947@yandex.ru
• Лычкова Алла Эдуардовна, д.м.н., заведующая отделом по патентной и изобретательской работе, Московский клинический научно-практический центр имени А.С. Логинова; 111123, Россия, Москва, шоссе Энтузиастов, д. 86; https://orcid.org/0000-0002-3856-275X; a.lychkova@mknc.ru



